2021年8月18日,中國醫學科學院阜外醫院胡盛壽院士、潘湘斌教授團隊成功為兩例三尖瓣返流患者完成LuX-Valve瓣膜植入手術。 至此,由健世科技自主研發的全球創新產品LuX-Valve瓣膜完成了確證性臨床試驗的全部患者入組。
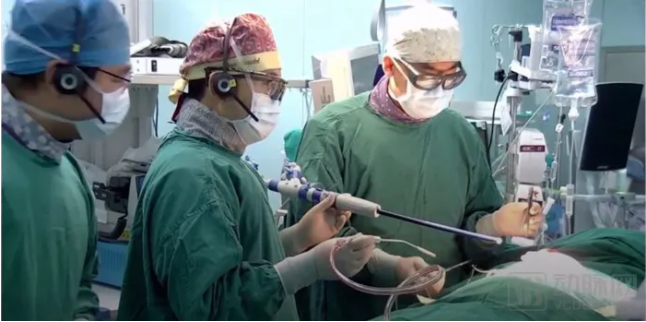
潘湘斌教授在進行三尖瓣LuX-Valve瓣膜植入手術
LuX-Valve分別開展了可行性臨床試驗和確證性臨床試驗,整個過程歷經數月,參研各單位和專家攻堅克難,勇於探索,建立了中國首創版的術前、術中、術後SOP,積累了豐富的經導管三尖瓣介入置換經驗,為LuX-Valve走向全球奠定了堅實的基礎。 LuX-Valve成功完成注册臨床試驗入組,標誌著中國經導管三尖瓣介入置換瓣膜產品和治療科技已走在世界前列!
國內八家頂級醫療機構參與了此次確證性臨床試驗,除前述胡盛壽院士、潘湘斌教授團隊外,還包括上海長海醫院徐志雲主任、陸方林教授團隊; 首都醫科大學附屬北京安貞醫院孟旭主任、張海波教授團隊; 華中科技大學同濟醫學院附屬協和醫院董念國主任、尚小珂教授團隊; 四川大學華西醫院郭應强教授團隊、陳茂教授團隊; 中國人民解放軍空軍軍醫大學第一附屬醫院楊劍教授團隊; 廣東省人民醫院郭惠明教授團隊; 浙江大學醫學院附屬第二醫院王建安書記、劉先寶教授團隊。
三尖瓣返流是臨床亟待解决的問題之一
三尖瓣瓣膜病是最常見的心臟疾病之一,因起病隱匿,初期臨床症狀得不到重視而被稱為“被遺忘的瓣膜”。 臨床上三尖瓣返流較狹窄較為常見,而且這類患者數量龐大。 由於三尖瓣無法完全關閉,導致心臟收縮期血液從右心室倒流至右心房。 長期來看,三尖瓣返流會導致心力衰竭,症狀包括外周水腫、腹水及肝部病變。
全球中度至重度三尖瓣返流患者人數由2016年4660萬人新增至2020年5060萬人,且預期於2030年增至6070萬人。 中國中度至重度三尖瓣返流患者人數由2016年860萬人增至2020年920萬人,且預期於2030年增至1060萬人。 三尖瓣患者生活質量低,死亡率高(約36%的嚴重三尖瓣返流患者在確診一年後去世,而約47.8%患者在確診5年後去世),囙此,治療三尖瓣返流已成為臨床亟待解决的熱點問題之一。
儘管三尖瓣返流情况普遍,但現時暫無獲批治療三尖瓣返流的經導管介入產品。 臨床研究中,三尖瓣返流的經導管介入治療有瓣膜修復和瓣膜置換兩種方案,而與經導管三尖瓣修復相比,經導管三尖瓣置換的應用範圍更廣,可有效降低三尖瓣返流的嚴重程度。 囙此,健世科技將經導管三尖瓣置換產品作為重點突破方向。
全球首創LuX-Valve有望成為全球首款商業化的經導管三尖瓣介入置換產品
原創之路,註定不會一蹴而就。 LuX-Valve歷經長達八年的研發歷程,曾經歷過數十次動物試驗失敗,也曾經歷過前所未有的質疑。 健世科技團隊和合作臨床專家不畏艱難,越挫越勇,終有全球首創的“非徑向支撐力依賴“和“室間隔固定”的設計理念,很好地解决了三尖瓣特殊病理的結構差异大、定位固定難和右心組織易損傷等問題。
2018年9月22日,長海醫院徐志雲團隊實現LuX-Valve經導管三尖瓣置換系統首例救治臨床人體應用,患者隨訪已近三年,現時生活狀況良好; 2020年6月16日由北京阜外醫院胡盛壽院士團隊實現首例可行性臨床研究首例人體應用; 2020年9月,完成可行性臨床試驗,檢驗結果初步已展現產品安全及有效,根據可行性臨床試驗結果,全因死亡率於出院時為零及於30天時為零; 2020年10月確證性臨床試驗在全國八家著名臨床中心全面開展; 2021年8月18日完成確證性臨床試驗入組。 回顧LuX-Valve的臨床試驗歷程,雖歷經艱辛,但漂亮的臨床結果與數據始終如一。
LuX-Valve注册臨床試驗順利完成入組,預示著產品商業化又邁進一大步。 據瞭解,現時全球範圍內,尚沒有同類產品完成此類試驗,LuX-Valve有望成為全球首款商業化的經導管三尖瓣介入置換產品。

LuX-Valve產品瓣膜
健世科技儲備豐富的結構性心臟病介入治療產品管線,即將讓更多患者獲益
LuX-Valve僅是健世科技結構性心臟疾病領域代表性產品之一,其自主研發的經導管主動脈瓣置換系統Ken-Valve也在同步進行注册臨床試驗。 此外,健世科技圍繞結構性心臟病領域的介入治療儲備了完整的創新技術和產品,二代經導管三尖瓣置換系統LuX-Valve Plus、經導管二尖瓣修復系統MitraPatch、經導管二尖瓣瓣膜夾及其輸送系統JensClip、心房間隔支架系統MicroFlux等產品已完成臨床試驗前的研發工作,正處於臨床前準備階段, 未來也將陸續分別應用於臨床。
健世科技依託其强大的自主研發和創新技術平臺,堅持“人無我有、人有我優“的產品戰略和“研發一代、儲備一代”的研發策略,深耕結構性心臟病介入治療各細分市場,全方位佈局差异化的產品管線。 隨著健世科技創新性產品的不斷推出,將為更多的結構性心臟病患者帶來福音。













